
「2023衡中同卷押题试卷二 答案」衡中同卷押题卷一,目前我们已经整理了「2023衡中同卷押题试卷二 答案」衡中同卷押题卷一的各科答案和试卷,更多衡中同卷请关注本网站。




19.(12分)(1)降低活化能(1分)②(1分)一112(1分)》(2)B(2分)(3)①1:2(2分)②随着温度升高,温度对平衡起决定作用,投料比对平衡影响逐渐减小(2分)③2(2分)④向左进行(1分)【解析】(1)分析反应历程可知,O作总反应的催化剂,从能量角度分析,它降低了反应的活化能。活化能较大的反应速率较小,故反应②控制总反应速率。反应②的反应热等于产物的相对能量总和与反应物的相对能量总和之差,△H2=(486十0一429一99)kJ·mol-1=一42kJ·mol1。根据盖斯定律,②×2+①得总反应,△H=2△H2+△H1,△H1=△H-2△H2=(-196+12×2)kJ·mol-1=-112kJ·mol-1。(2)该反应是气体分子数减小的反应,甲容器平衡时,气体分子数减小,总压强减小;以甲容器为参照,甲容器缩小体积(加压)转化成乙容器,加压,平衡向正反应方向移动。温度不变,平衡常数不变,A项错误;平衡向右移动,SO2的平衡转化率增大,B项正确;平衡时,乙容器中SO3浓度较大,C项错误;混合气体总质量不变,气体总物质的量减小,相对分子质量增大,D项错误。(3)①相同温度下,投料比越大,SO2平衡转化率越大,x1代表的投料比为1:2。②该反应的正反应是放热反应,升高温度平衡向逆反应方向移动,SO2的平衡转化率减小,当温度升高到一定程度,投料比对SO2的平衡转化率影响逐渐减小,故三种投料比的SO2平衡转化率趋向相等。③x3代表投料比为2:1。对应SO2的平衡转化率为80%,设起始投入c(O2)=2mol·L-1,c(S02)=1mol·L1,列“三段式”:2S02(g)十02(g)→2S03(g)起始/(mol·L1)120转化/(mol·L-1)0.80.40.8平衡/(mol·L-1)0.21.60.80.2p(SO2)=1.3 MPa X0.2+1.6+0.8=0.1MPa,b(O2)=0.8MPa,p(SO3)=0.4MPa。由标准分压pP°=号,=10kPa知,p(S0)=81Mg=1,0.1 MPap°(O2)=8,p°(SO3)=4。标准平衡常数K⊙[p°(SO3)]242Lb(S02)]2·p(O2)8X12=2。32④Q=12X2=4.5>K6,反应向左进行。

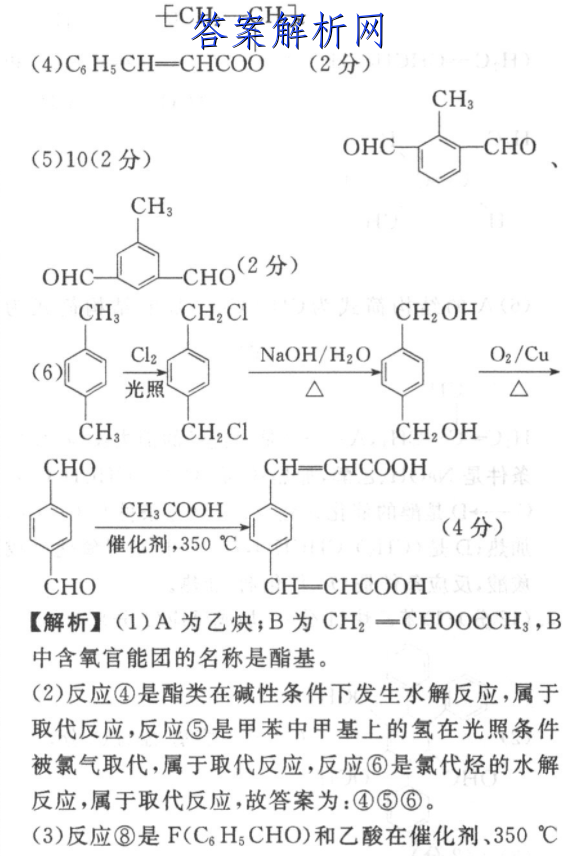

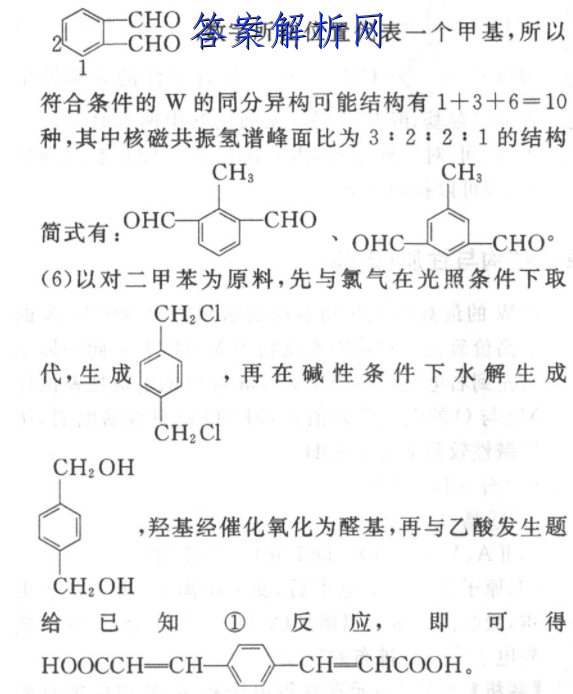
6.(16分)(1)乙炔(1分)酯基(1分)(2)④⑤®(2分)催化剂,350℃(3)CH;CHO CH COOHC Hs CH-CHCOOH+H2O(2ECH2一CH3n(4)C H;CH-CHCOO(2分)》CH3(5)10(2分)OHCCHOCH3OHC-CHO(2分)CH;CH2 CICH2 OHCl2NaOH/H2OO2/Cu(6)光照△△CH3CH2 CICH2 OHCHOCH-CHCOOHCH3 COOH(4分)催化剂,350℃CHOCH-CHCOOH【解析】(1)A为乙炔;B为CH2一CHOOCCH3,B中含氧官能团的名称是酯基。(2)反应④是酯类在碱性条件下发生水解反应,属于取代反应,反应⑤是甲苯中甲基上的氢在光照条件被氯气取代,属于取代反应,反应⑥是氯代烃的水解反应,属于取代反应,故答案为:④⑤⑥。(3)反应⑧是F(C6HCHO)和乙酸在催化剂、350℃条件下发生题给反应①的反应,方程式为:催化剂,350℃C&Hs CHO十CH COOHCHCH-CHCOOH+H2O。ECH2一CH(4)H的结构简式为C6HsCH=CHCOO(5)G为C6HCH=CHCOOH,W为只有一种官能团的芳香化合物,W能发生银镜反应,且含有2个氧原子,不饱和度为6,说明W中含有2个醛基,同时还有一个饱和碳原子,若苯环上只有一个取代基结CHOCHCHO构简式为:〔,若苯环上有2个取代基结构简CH2 CHO式可能为:,还可以是邻位和间位,共3CHO种,若苯环上有3个取代基结构简式可能有6种,分别为:OHC〔CHOOHCCHOCHOCHO,数字所在位置代表一个甲基,所以符合条件的W的同分异构可能结构有1十3+6=10种,其中核磁共振氢谱峰面比为3:2:2:1的结构CH3CH:简式有:OHC、OHCCHOCHO(6)以对二甲苯为原料,先与氯气在光照条件下取CH2 CI代,生成,再在碱性条件下水解生成CH2 CICH2 OH,羟基经催化氧化为醛基,再与乙酸发生题CH2 OH给已知反应,即可得HOOCCH-CH-CH-CHCOOH.




评论